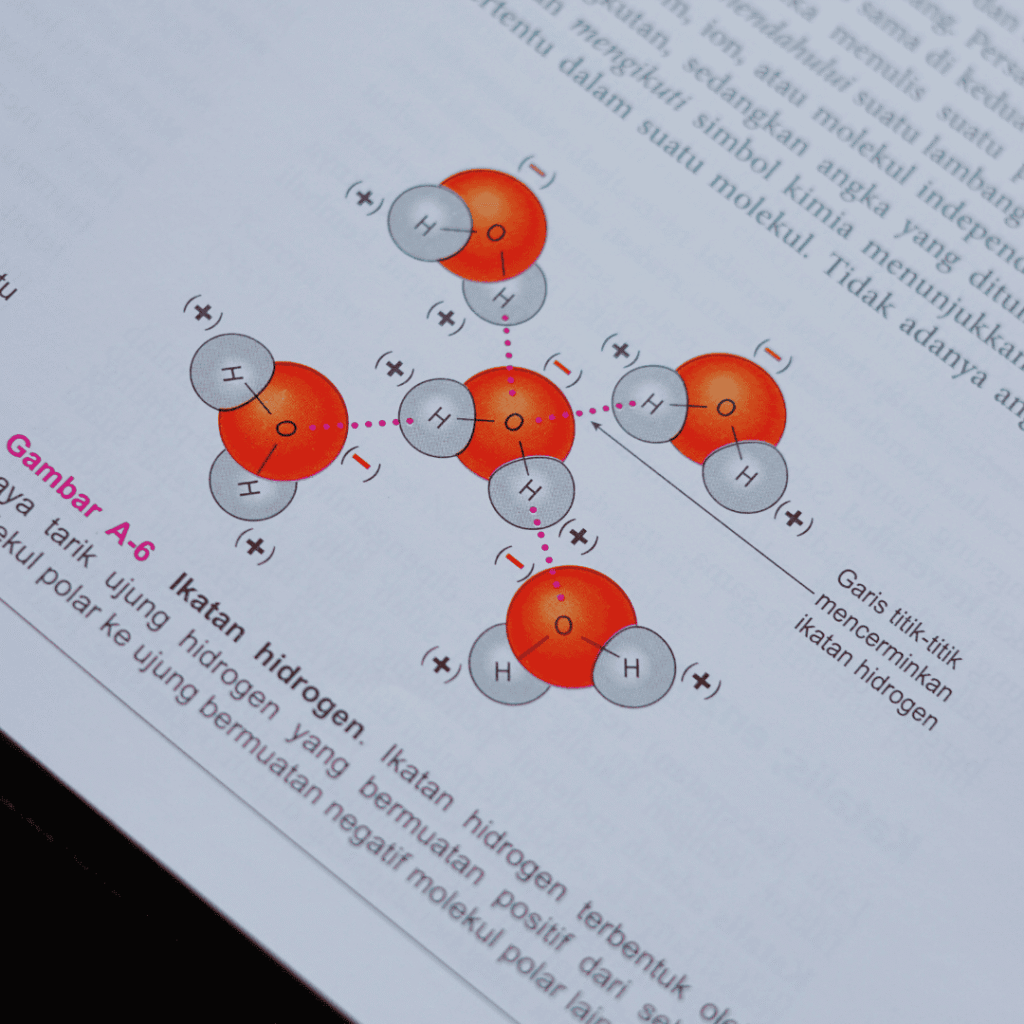
O vodíkové vazbě jsme se učili na základní škole v hodinách chemie. Poučka zněla: Vodíková vazba je interakce mezi atomem vodíku jedné molekuly a elektronegativním prvkem z jiné molekuly [1]. Nejlepším příkladem je kapalná voda, kde vodíkové vazby vznikají mezi atomy vodíku a kyslíku. Je to právě vodíková vazba, která propůjčuje vodě její vlastnosti, například extrémně vysoký bod varu.
Ze spektroskopických měření víme, že přítomnost vodíkových vazeb vede k posunu spektrálních pásů [2]. Typicky se spektrální pásy posunou k nižším energiím, čemuž říkáme červený posuv. Proč? Přítomnost vodíkové vazby natáhne kovalentní vazbu mezi vodíkem a atomem, ke kterému je vodík vázán (ve vodě se jedná o vodík a kyslík). Natažení vazby znamená, že potřebujeme méně energie na její rozvibrování. To si můžeme představit tak, že u vytahané pružiny je také potřeba méně energie na její rozkmitání. Ovšem existuje i situace, kdy v důsledku vodíkové vazby dojde ke zkrácení příslušné kovalentní vazby, a proto se spektrální pásy posunou k vyšším energiím: hovoříme o modrém posuvu. Pro tuto situaci navrhli čeští vědci označení „nepravá vodíková vazba“, které se však nikdy neujalo [2].
Ti samí vědci nedávno objevili, že vodíkové vazby mohou vzniknout i mezi vodíkem a elektropozitivním prvkem [3]! A právě o tom je i vámi citovaný článek na iRozhlasu. Na základě svého objevu vědci navrhují úpravu zmiňované poučky o vodíkové vazbě tak, aby zahrnovala i situace, kdy vodík vytváří vodíkovou vazbu s elektropozitivním prvkem, ale o „nepravé“ vodíkové vazbě se nezmiňují.
Závěrem můžeme shrnout, že podle současného poznání dochází ke vzniku vodíkové vazby mezi vodíkem a libovolným těžším prvkem periodické tabulky, bez ohledu na jeho afinitu k elektronům (ochota prvku stávat se záporně nabitým). To vede k úpravě našeho pohledu na tuto velmi důležitou interakci a zobecnění její definice. Vodíkové vazby se spektroskopicky projeví posunem pásů. Tento posun může být buď k vyšším, nebo nižší energiím, podle toho, jestli dojde ke zkrácení, nebo natažení příslušné kovalentní vazby vodíku. Nakonec je třeba zmínit, že vodíková vazba, ať už jakákoliv, je jen speciálním označením nekovalentních interakcí [4] mezi vodíkem a ostatními prvky. Tak můstkům zdar!
Pro Zeptej se vědce odpovídal Vítek
Zdroje:
[1] https://cs.wikipedia.org/wiki/Vod%C3%ADkov%C3%A1_vazba
[2] http://www.chemicke-listy.cz/docs/full/2008_10_884-888.pdf