Nejdříve se podívejme na strukturu kapalin. Kapaliny jsou tvořeny částicemi, které na sebe navzájem působí – v případě vody se tedy jedná o jednotlivé molekuly H₂O. Nyní se zaměřme na jednu konkrétní molekulu vody: můžeme si představit, že všechny okolní molekuly ji k sobě přitahují. Uvnitř kapaliny jsou molekuly obklopeny ze všech stran a tyto síly se navzájem vyruší. Jiná situace však nastává pro molekuly na povrchu. V takovém případě působí síla směrem dovnitř kapaliny, protože v tomto směru se vyskytuje mnohem více molekul, než je v okolí molekul plynu. Kapaliny jsou mnohem více husté a z hustoty a molekulové hmotnosti můžeme vypočítat, že na téměř 1300 molekul vody připadá pouze jedna molekula vzduchu. Výsledkem tohoto působení je, že molekuly na povrchu jsou vtahovány dovnitř a vytvářejí tak pružnou blánu, která se vodu snaží smrštit. Kapaliny se proto snaží získat co nejmenší povrch – a takovým tvarem je koule. Toto tzv. povrchové napětí umožňuje mnoho krásných přírodních jevů jako pohyb vodoměrek po hladině nebo mýdlové bubliny či rosu.
Důvodem, proč kapalina nesteče dolů přes hranu, je právě povrchové napětí. Blána povrchového napětí smršťuje kapalinu a nedovoluje jí zvětšit svůj povrch a přetéct. Podobný jev nastane, když do skleničky nalijeme příliš mnoho vody a z boku můžeme pozorovat, že voda přesahuje okraj sklenice. Pokud budeme dále přidávat kapky vody, nalezneme okamžik, kdy se síly vyrovnají a voda přece jen přeteče.
Nyní už víme, co je původcem povrchového napětí a proč voda nepřeteče přes stůl, ale zbývá ještě objasnit, co může tento jev ovlivňovat. Povrchové napětí závisí na mezimolekulových interakcích (působení molekul na sebe navzájem). Z toho plyne, že každá kapalina bude mít jiné povrchové napětí a důležitým parametrem je tedy její složení a případné nečistoty či příměsi. Například tzv. povrchově aktivní látky (surfaktanty nebo tenzidy) mají schopnost se hromadit na povrchu a snižovat právě povrchové napětí [1]. Látky s těmito vlastnostmi se tak často používají v čisticích a pracích prostředcích, protože pak voda lépe smáčí znečištěný povrch, rychleji rozpouští špínu a smývá ji.
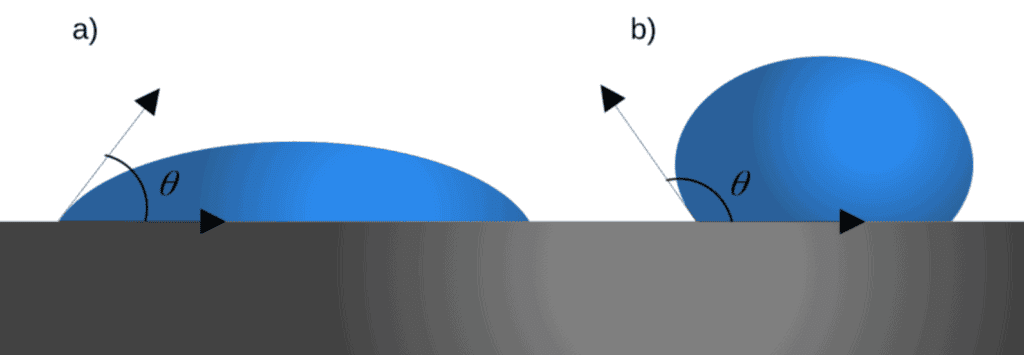
S povrchem kapaliny interagují molekuly plynu v jeho okolí a také pevná látka, která tvoří stůl. Výsledkem těchto působení je další vlastnost kapalin, tzv. smáčivost, kterou charakterizuje kontaktní úhel θ (neboli úhel smáčení, značený řeckým písmenem theta; viz obrázek). Čím větší úhel, tím méně bude kapalina na daném povrchu smáčivá – bude se ho štítit (obrázek b) a snáze steče. To nastává v případě vodoodpudivých materiálů, např. teflon nebo Gore-Tex [2].
Teplota je dalším důležitým faktorem ovlivňujícím povrchové napětí: s rostoucí teplotou povrchové napětí klesá [3]. Nakonec jako možné faktory zmiňme také vnější síly působící na kapalinu jako proudění nebo odpor vzduchu, který deformuje padající dešťové kapky a ty tak nemohou mít symetrický, kulový tvar.
Pro Zeptej se vědce odpovídal Jakub
Zdroje:
[1] Sedlaříková, J.: Chemie a technologie tenzidů II http://kosmetika.ft.utb.cz/Services/Downloader.ashx?id=134&disposition=inline

